El cefepima es un antibiótico betalactámico utilizado para combatir infecciones nosocomiales, infecciones de vías respiratorias inferiores incluyendo la neumonía y la bronquitis, así como también las infecciones urinarias y otras más. Consulte a su médico antes de utilizar o consumir este medicamento.
Cefepima
Nombre comercial
El nombre comercial del principio activo cefepima es Maxipime®.
La presentación de este fármaco se puede encontrar en polvo para solución inyectable. Se distribuye con preferencia para uso exclusivo de centros de salud.
En otro países
En otros países el nombre del fármaco puede hallarse de la siguiente forma:
Alemania: Maxipime
Argelia: Axepim
Argentina: Cefepime
Bélgica: Cefepim
Brasil: Cefalospim
Canadá: Cefepime
Chile: Cefepima
Colombia: Cefdeltime
Dinamarca: Maxipime
EEUU: Cefepime
Egipto: Cefepime
Emiratos árabes: Maxipime
España: Cefepima
Estado del vaticano: Cefepime
Finlandia: Maxipime
Francia: Axepim
Grecia: Maxipime
India: C pime
Irán: Cefemax
Italia: Maxipime
Malasia: Maxipime
México:Baxypime
Nueva Zelanda:
Perú: Cepimcef
Polonia: Maxipime
Portugal: Maxipime
Rumania: Cefepima
Suiza: Cefepime
Turquía: Avipim
Venezuela: Aspime
Forma farmacéutica
Cada frasco con solución inyectable contiene:
Clorhidrato monohidratado de cefepima equivalente a 500 mg, 1 g de cefepima.
Excipiente, c.b.p.
Cada ampolleta con diluyente contiene agua inyectable 3, 5 y 10 ml.
Vía parenteral
¿Qué es la cefepima?
La Cefepima o también llamada cefepime, se comercializó en 1994, es un antibiótico del grupo de las cefalosporinas y se clasifica de cuarta generación.
La cefepima tiene propiedades bactericidas sobre microorganismos gram negativos, gram positivos y enterobacteriaceae, como providencia, citrobacter freundii, serratia, morganella. streptococcus pneumoniae, enterobacter aerogenes, pseudomonas aeruginosa, staphylococcus aureus, enterobacter cloacae.
La cefepima es un antibiótico utilizado para combatir de infecciones graves. Es bien tolerado y la incidencia de efectos adversos graves es menor en comparación con otros antibióticos. Como consecuencia a que su excreción es predominantemente por el riñón, su vida media se extiende específicamente en presencia de fallas renales, por lo que es necesario ajustar la dosis cuando la filtración glomerular es menor de 50 mL/min
Cefepima
Composición y preparación
La composición de la cefepima se puede hallar en frasco-ampolla para una sola dosis, en presentación de 1 gramo y de 2 gramos.
El polvo de la cefepima se mezcla con preparaciones inyectables para administrar como solución inyectable en vena (intravenosa) o una perfusión (goteo). (Ver artículo: Gentamicina)
Mecanismo de acción
El mecanismo de acción de la cefepima reside en inhibir la síntesis de la pared celular bacteriana, a la que se une por su alta correspondencia con las proteínas ligadoras de penicilina.
Algunas cefalosporinas son degradadas por múltiples betalactamasas mediadas por plásmidos y cromosomas, pero no ocurre con la cefepima, de hecho muestra más actividad frente a cocos grampositivos.
La cefepima es efectiva sobre cepas generadoras de betalactamasas como por ejemplo: Enterobacteriaceae, responsables de sepsis graves, y con resistencia a los antibióticos tradicionales.
Por lo que su utilización debe hacerse con preferencia a nivel intrahospitalario. La cefepima se administra por vía intravenosa.
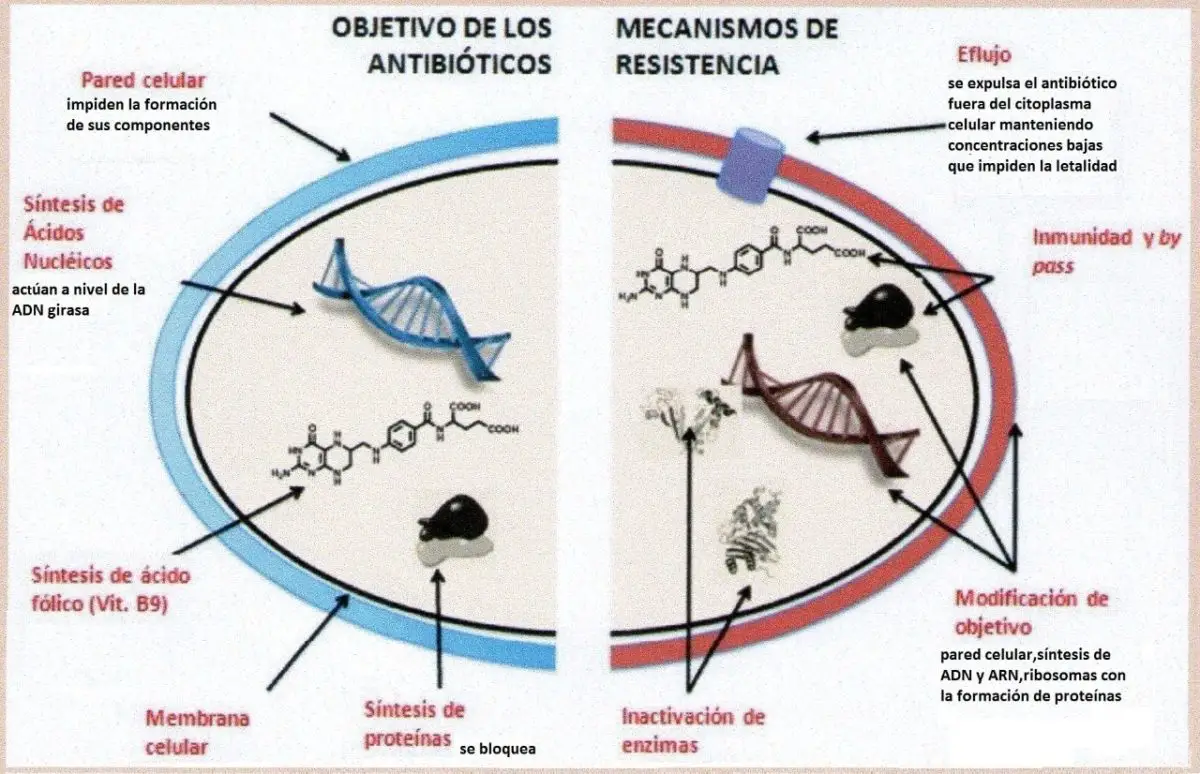
Mecanismos de acción de los antibióticos
Indicaciones
La cefepima está indicada para el tratamiento de las siguientes infecciones:
• Bronquitis y neumonía entre otras infecciones de las vías respiratorias.
• Infecciones de las vías urinarias tanto las complicadas como las no complicadas, inclusive pielonefritis.
• Las infecciones de la piel.
• Las infecciones intraabdominales, inclusive peritonitis.
• Infecciones de las vías biliares.
• Profilaxis en cirugías abdominales
• Septicemia.
• Meningitis bacteriana.
• Tratamiento empírico de la neutropenia febril.
• Infecciones ginecológicas.
•Endocarditis (infección de las válvulas y revestimiento del corazón)
• Meningitis (infección de las membranas que recubren el cerebro y la columna)
• Infecciones en la sangre.
Endocarditis
Dosis
Cefepima es administrada por:
• Por perfusión (goteo) en vena (perfusión intravenosa).
• Por inyección lenta en vena (intravenosa)

Perfusión intravenosa
La dosificación dependerá del tipo y grado de la infección. Así como también de la edad, del peso y del funcionamiento renal del paciente a ser tratado.
La cefepima se administra de dos a tres veces al día, la dosis recomendada es:
Dosis para adultos y adolescentes
• Adultos y adolescentes (12 años en adelante) es de 4 a 6 gramos al día,
El tratamiento requiere ser suministrado por un lapso aproximado de 7 a 10 días. Las infecciones más severas podrían necesitar un tratamiento más extenso.
En el caso de profilaxis en cirugía abdominal en adultos se recomienda la dosis 60 minutos antes de iniciar la cirugía se debe indicar una dosis de 2 g de cefepima por in¬fusión durante media hora, inmediatamente 500 mg de metronidazol.
Profilaxis en cirugía abdominal
Es importante acotar que la dosis de metronidazol debe ser preparada y administrada de acuerdo a las indicaciones para este producto. Ya que, por la incompatibilidad, entre cefepima y metronidazol no deben ser mezclados en el mismo contenedor.
Es aconsejable drenar la línea intravenosa con un fluido compatible, antes de la infusión del metronidazol. Si la cirugía tiene una duración de más de doce horas, se debe iniciar su administración con la segunda dosis de ambos productos, doce horas después de la administración inicial.
Dosis pediátricas
• En el caso de pacientes pediátricos con funcionamiento renal normal, de 1 mes de nacidos hasta los 12 años, se recomienda para tratar infecciones de las vías urinarias, neumonía o infecciones de la piel la siguiente dosis:
En pacientes mayores de 2 meses de edad con un peso menor o igual a 40 kg: 50 mg/kg cada 12 horas por un periodo de 10 días. Para atender infecciones más severas puede indicarse cada 8 horas.
• En el caso de presentarse septicemia o meningitis bacteriana en pacientes mayores de 2 meses de edad con un peso menor o igual a 40 kg: 50 mg/kg cada 8 horas por un periodo de 7 a 10 días. Se recomienda la siguiente dosis:
En pacientes mayores de 2 meses de edad, se sugiere indicar una dosis de 30 mg/kg cada 12 horas o cada 8 horas.
• En el caso de pacientes con insuficiencia renal la cefepima, hay que ajustarla para compensar la menor velocidad de eliminación renal. Se recomienda la siguiente dosis:
La dosis de inicio de cefepima para paciente inicial, que padecen alteración renal moderada es la misma que se administra a los pacientes con función renal normal.
A los pacientes en hemodiálisis que reciben cefepima, se le debe tratar de la siguiente manera: 1 g de dosis inicial de carga en el primer día de tratamiento, luego de 500 mg diarios.
Para los días en que se realiza diálisis, se debe indicar la administración de cefepima luego de la diálisis y preferiblemente tomarse en el mismo horario diariamente durante la duración del tratamiento.
En los pacientes sometidos a hemodiálisis, alrededor del 68% de la cefepima que se mantiene en el organismo al iniciar la diálisis será eliminado en un tiempo de 3 horas de diálisis.
En los pacientes que reciben diálisis peritoneal continua ambulatoria, debe recibir la dosis recomendada para pacientes con función renal normal, que es 500 mg, 1 ó 2 g dependiendo del grado de infección y con un intervalo de cada 48 horas.
Diálisis peritoneal
Las personas con insuficiencia renal, debe realizarse un ajuste de la dosis de cefepima en los pacientes pediátricos, debido a que la excreción urinaria es la ruta de eliminación primaria. En pacientes menores de 12 años de edad con insuficiencia renal, se indica una dosis de 50 mg/kg en los pacientes de 2 meses hasta 12 años de edad, se recomienda una dosis de 30 mg/kg en los pacientes de 1 a 2 meses de edad, son comparables con una dosis de 2 g en un adulto.
En los pacientes con insuficiencia hepática no es necesario ajustes de la dosis.
Precauciones
Antes de recibir el tratamiento con cefepima conviene informar al médico tratante si es alérgico a:
• Cefepima
• Los antibióticos de carbapenem o a los antibióticos de penicilina
• Así como también a los antibióticos de cefalosporina como cefaclor, cefprozil, ceftarolina, cefadroxilo, cefazolina, cefdinir, cefixima, cefotaxima, cefotetan, cefoxitina, ceftibuten, ceftriaxona, cefpodoxima, ceftazidima, cefditoren, cefuroxima y cefalexina.
• Cualquier otro fármaco que le produzca alguna reacción alérgica.
Informe al médico tratante si está consumiendo suplementos nutricionales, vitaminas u otros fármacos con o sin receta médica.
Indique al médico tratante si tiene alguna enfermedad de tipo gastrointestinal, colitis, enfermedad hepática o enfermedad renal.
Informe al médico tratante si está embarazada o está en periodo de lactancia.

Algunos fármacos podrían llegar a ocasionar problemas de salud en los bebés, incluso si fueron consumidas en pequeñas cantidades. Es por esto que es recomendable que, si estas lactando y alimentando a tú bebé, no ingiera ningún medicamento sin consultar antes con un médico. El especialista le informará si es necesario suspender la lactancia.
Durante el tratamiento con cefepima, si es diabético y hace una prueba de glucosa en la orina, se recomienda usar Clinistix o TesTape. No use Clinitest, para examinar el nivel de azúcar en su orina mientras recibe este medicamento.
Cumpla las recomendaciones médicas. Ya que, su médico podría indicar algunas pruebas de laboratorio para comprobar la respuesta de su organismo a la inyección de cefepima.
Reacciones adversas
Cualquier medicamento puede producir efectos adversos, eso no quiere decir, que todas las personas los sufran.
En el caso de la cefepima, se podrían presentan algunos de los siguientes efectos secundarios:
• Colitis pseudomembranosa (inflamación del intestino grueso) produce diarrea acuosa con calambres abdominales y fiebre (probabilidad de padecer este efecto secundario: 1 de cada100 personas).
• Anafilaxis (pérdida de la conciencia) presenta dificultad para respirar, inflamación de la cara o cuerpo, erupción, desmayo (probabilidad de padecer este efecto secundario: 1 de cada 1.000 personas).
• Eritema multiforme (erupción cutánea) se puede presentar de forma leve o moderada con presencia de erosiones y ampollas (probabilidad de padecer este efecto secundario: la frecuencia no puede ser estimada a partir de los datos disponibles).
• Síndrome de Stevens-Johnson, se presenta con un inicio repentino de erupción e inflamación aguda con presencia de ampollas o descamaciones de la piel, asociada a fiebre alta y con dolor en las articulaciones. (probabilidad de padecer este efecto secundario: 1 a 10 personas de cada 10.000).
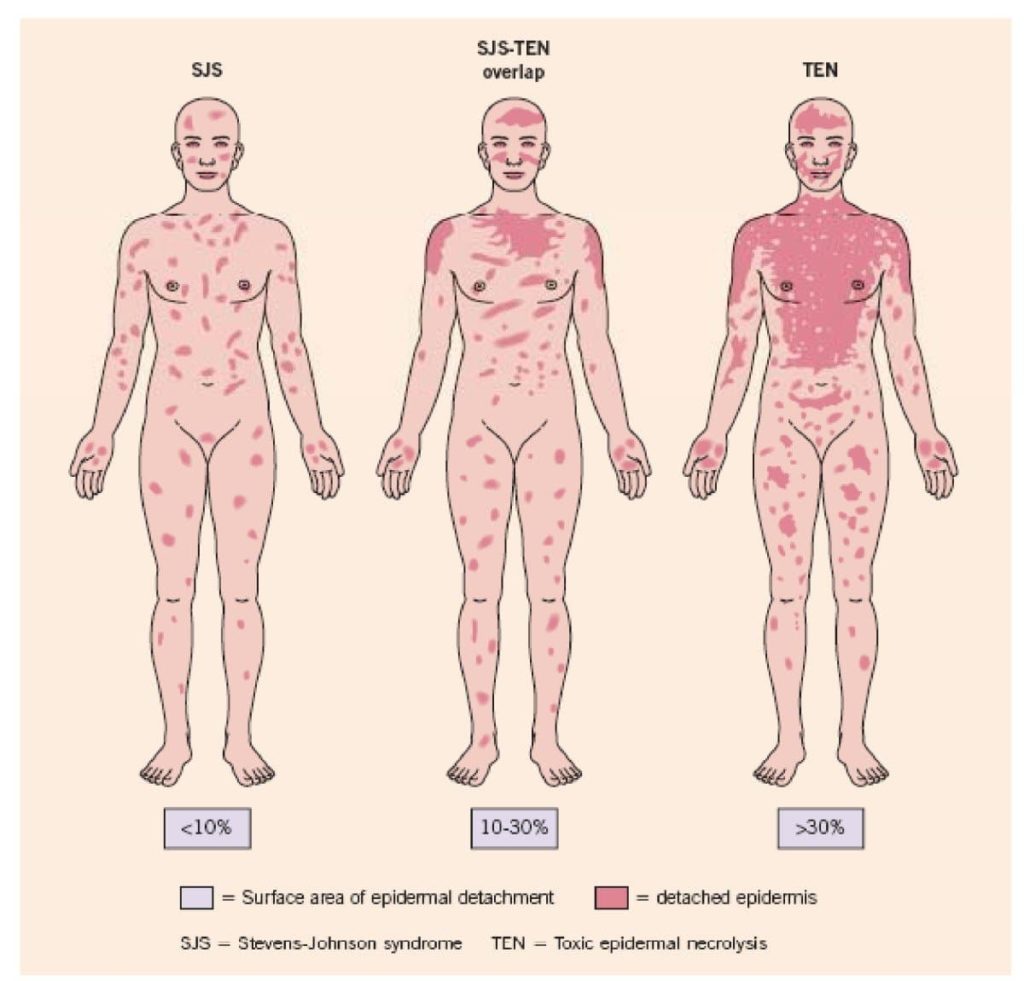
El Síndrome de Stevens Johnson es una enfermedad inflamatoria aguda, que tiene como efecto causar una reacción de hipersensibilidad, en forma de eritema multiforme que afecta principalmente la piel, las mucosas y en ocasiones a órganos internos. Inicia por repentina de lesiones cutáneas con vesículas centrales, en piel y mucosas.
También se pueden presentar los siguientes efectos secundarios con probabilidad de frecuencia de 1 de cada 10 personas:
• Alteraciones en los resultados de laboratorios para anticuerpos que causan la destrucción de glóbulos rojos.
• Reacciones alérgicas en la piel.
• Diarrea.
• Dificultades respiratorias.
• En el área de inyección se puede presentar: dolor, hinchazón e irritación.
• Flebitis.
• Alteración del recuento sanguíneo, incluyendo bajo número de glóbulos rojos y leucocitos.
• Error de valores de laboratorio que señalan insuficiencia hepática.
Otros efectos secundarios con probabilidad de frecuencia de 1 de cada 100 personas:
• Dolor de cabeza
• Fiebre
• Piel irritada, urticaria (Ver artículo de: Celestamine)
• Aumento de algunos resultados de análisis de sangre: urea y creatinina.
• Inflamación de la vagina
• Náuseas y vómitos
• Inflamación del área de perfusión
• Llagas superficiales y pequeñas dentro de la boca y en la base de las encías
• Alteraciones del recuento sanguíneo de leucocitos y plaquetas.
Otros efectos secundarios que son considerados raros con probabilidad de frecuencia de 1 de cada 1000 personas:
• Trastorno de la percepción.
• Confusión o mareo.
• Alteración del apetito.
• Ataque epiléptico.
• Dificultades respiratorias.
• Escalofríos.
• Dolor abdominal.
• Estreñimiento.
• Ensanchamiento de vasos sanguíneos.
Otros efectos secundarios no conocidos (la probabilidad de frecuencia no puede calcularse a partir de los datos disponibles):
• Shock anafiláctico potencialmente mortal.
• Alteración del recuento sanguíneo, disminución aguda de glóbulos rojos o glóbulos blancos.
• Disfunción cerebral
• Sangrado de vasos sanguíneos dañados
• Confusión alucinaciones.
• Movimientos de los músculos
• Insuficiencia renal
• Trastorno funcional del estómago y el intestino
Insuficiencia renal
En el caso que experimente cualquier síntoma de efecto adverso, consulte de inmediato a su médico tratante, incluso si se trata de posibles efectos adversos que no hayan sido descritos.
Recomendaciones para administrar la cefepima
La administración intravenosa (I.V.)
Con infecciones severas o donde este en riesgo la vida, debe reconstituirse la cefepima con agua inyectable estéril, con inyección de dextrosa al 5%, o con solución salina al 0.9% utilizando los volúmenes de diluyentes correspondientes.
La solución se debe inyecta de manera directa en la vena, en un periodo de 3 a 5 minutos o en la sonda del equipo de administración, mientras el paciente recibe una solución I.V. compatible.
La administración intramuscular (I.M.)
La cefepima puede reconstituirse con solución salina al 0.9%, agua inyectable estéril, dextrosa al 5% o agua inyectable bacteriostática con parabenos o alcohol bencílico, y luego administrarse mediante inyección intramuscular.
Inyección Intramuscular
Los fármacos parenterales, deben examinarse a simple vista con el objeto de detectar la presencia de partículas antes de su administración; no debe usarse cuando se detectan partículas.
¿Cómo conservar la cefepima?
La cefepima al igual que el resto de los medicamentos, debe mantenerse fuera del alcance de los niños. No debe usarlo después de la fecha de caducidad que indica el fármaco.
Conservar el medicamento a temperatura ambiente a no más de 30°C o 7 días en refrigeración, 2-8°C.
Descarte la cefepima si observa que la solución está turbia y descolorida; la condición debe ser transparente y entre incolora y amarilla ámbar.
Hecha la mezcla, el producto se conserva 24 horas, desechar cualquier solución no utilizada en ese periodo de tiempo. La solución con cefepima en polvo, debe usarse de inmediato.
https://www.youtube.com/watch?v=O_LwgIx-ndM
Propiedades farmacodinámicas
El mecanismo de acción de la cefepima provoca una acción bactericida, se basa en la inhibición de la síntesis de la pared bacteriana debido a la inhibición de las proteínas.
La eficacia depende en gran medida del tiempo en el que los niveles del fármaco prevalecen en la concentración inhibitoria mínima del patógeno involucrado.
La cefepima tiene una afinidad reducida a las betalactamasas, codificadas por cromosomas y es muy resistente a la hidrólisis de la mayoría de betalactamasas.
La resistencia puede deberse a los siguientes mecanismos:
• Impermeabilidad de la membrana externa, lo que restringe el acceso de la cefepima a las proteínas de unión a la penicilina en organismos gran negativos.
• Afinidad reducida de las proteínas de unión a la penicilina y la cefepima.
• Producción de betalactamasas competentes de hidrolizar efectivamente la cefepima.
Propiedades farmacocinéticas
La cefepima posee las siguientes propiedades farmacocinéticas:
La cefepima es lineal dentro del intervalo de 250 mg a 2 g por vía intravenosa; no se diferencian en relación a la conservación del tratamiento.
Luego de la administración intravenosa de 2 g durante 30 minutos a personas voluntarias sanas, las concentraciones de absorción plasmáticas máximas (Cmax) fueron de 126 a 193 μg/ml.
La cefepima se distribuye de forma homogénea en los líquidos y los tejidos corporales. En el intervalo de 250 mg a 2 g, la distribución tisular relativa de la cefepima no varía en relación a la dosis tomada.
El volumen de distribución en el estado estacionario es de 18 l. No hay estudios que permitan confirmar la acumulación en voluntarios sanos cuando se administran dosis de hasta 2 g por vía intravenosa cada 8 horas durante 9 días. La unión a proteínas plasmásticas de cefepima es menor de 19 % y no depende de las concentraciones séricas. La semivida de eliminación media es de un promedio de 2 horas.
El metabolito urinario básico es el óxido N-metilpirrolidona, una amina terciaria, que solo supone alrededor del 7 % de la dosis. Por lo que la cefepima se metaboliza en una pequeña proporción.
El aclaramiento renal promediar de cefepima es de 110 ml/min; esto indica que la cefepima se elimina casi exclusivamente mediante mecanismos renales, principalmente por filtración glomerular. La recuperación en orina es de aproximadamente el 85 % de la dosis. Tras una administración intravenosa de 500 mg, la cefepima dejó de ser detectable en el plasma tras 12 horas y en la orina tras 16 horas.
En el caso de los pacientes de tercera edad: se realizaron estudios, donde se analizó la distribución de cefepima en pacientes masculinos y femeninos mayores de 65 años. La eficacia en pacientes de edad avanzada son comparables a las de los adultos, sin embargo se observó una ligera prolongación de la semivida de eliminación y unos valores menores de aclaramiento renal en pacientes de edad avanzada.
Por lo que se recomienda ajustar la dosis cuando se presente insuficiencia renal concomitante.
En el caso de la población pediátrica: se realizaron investigaciones donde se evaluó la farmacocinética de la cefepima en dosis únicas y múltiples en pacientes pediátricos de entre 2 meses y 16 años de edad. Se les administró dosis de 50 mg/kg mediante perfusión intravenosa; las dosis múltiples se administraron cada 8 o 12 horas durante 48 horas.
No debe suministrar antibiótico sin la prescripción del pediatra
Las concentraciones plasmáticas medias de cefepima, tras la primera dosis fueron similares al estado estacionario y se evidenció, una leve acumulación en la administración de las dosis adicionales.
En los bebés y niños, se observó tras la primera dosis en el estado estacionario, no variaron, independientemente de la periodicidad de administración cada 12 o 8 horas. No se evidenciaron diferencias farmacocinéticas en pacientes de distinta edad y distinto sexo.
Se pudo observar que después de la administración de una única dosis intravenosa, el aclaramiento total medio fue 3,3 ml/min/kg y el volumen de distribución 0,3 l/kg. La semivida de eliminación media total 1,7 horas. En el caso de la orina se recupera inalterada un 60,4% de cefepima de la dosis administrada y la principal via de eliminación fue la excreción renal con un valor medio de 2,0 ml/min/kg.
En investigaciones realizadas en casos de insuficiencia renal, en personas con diferentes grados de insuficiencia renal, han dejado evidenciar que se extiende la semivida de eliminación de manera significativa. Existe relación lineal entre el aclaramiento total, y el aclaramiento de creatinina (el torrente sanguíneo conduce la creatinina hacia los riñones, cuya función es extraerla de la sangre en el proceso de filtración y de expulsarla mediante la orina) en personas con insuficiencia renal.
La semivida de eliminación media, durante la hemodiálisis es de 13 horas y de 19 horas en diálisis peritoneal continua ambulatoria.

La creatinina es un producto de desecho, que elaboran los músculos a un ritmo constante como parte de la actividad diaria normal.
En cuanto a la insuficiencia hepática, la cinética de la cefepima se conserva invariable en pacientes con fibrosis quística e insuficiencia hepática cuando se suministra una dosis única 1 g. Por lo que, no se requiere ajustar la dosis.
Interacciones
No deben mezclarse las soluciones de cefepima con los siguientes fármacos:
• Metronidazol
• Vancomicina
• Gentamicina
• Sulfato de tobramicina
• Sulfato de netilmicina
Porque pueden surgir incompatibilidades tanto físicas como químicas. En caso de ser necesario indicarse un tratamiento concomitante, se deben administrar de forma separada.
La Cefepima puede hacer daño a los riñones, el riesgo puede aumentar si también usa ciertas otras medicinas, tales como:
• Antibióticos inyectables
• Antivirales
• Quimioterapia
• Medicina para los trastornos intestinales, para prevenir el rechazo de órgano trasplantado y dolor o la artritis (Tylenol, Advil, Aspirin y Aleve).
• Medicamentos inyectables para tratar la osteoporosis
No se puede tomar diuréticos o “pastillas para eliminar el agua” como furosemide, ya que, puede ocasionar interacciones con la cefepima.
La furosemida un diurético del grupo de las sulfonamidas. Aumenta la eliminación de orina (diurético) y reduciendo la presión arterial (antihipertensivo). Consulte a su médico antes de utilizar cualquier medicamento.
No consuma ningún medicamento sin receta o con recetar sin consultar antes con el médico tratante. Quien es el especialista indicado para sugerir el tratamiento correspondiente.
Contraindicaciones
La cefepima está contraindicada en pacientes que sufran reacciones de hipersensibilidad a cualquier componente de la fórmula, en este caso en específico a las cefalosporinas, penicilinas u otros antibióticos betalactámicos carbapenémicos y monobactámicos.
Debido a que la cefepima contiene L-arginina, este fármaco está contraindicado en pacientes con hipersensibilidad a la L-arginina y acidosis. Por lo que es recomendable tener precaución en casos de hiperpotasemia.
Sobredosis
En caso de sobredosis y específicamente en pacientes con insuficiencia renal, la hemodiálisis permitirá a eliminar la cefepima del organismo; pero en el caso de la diálisis peritoneal no resulta útil.
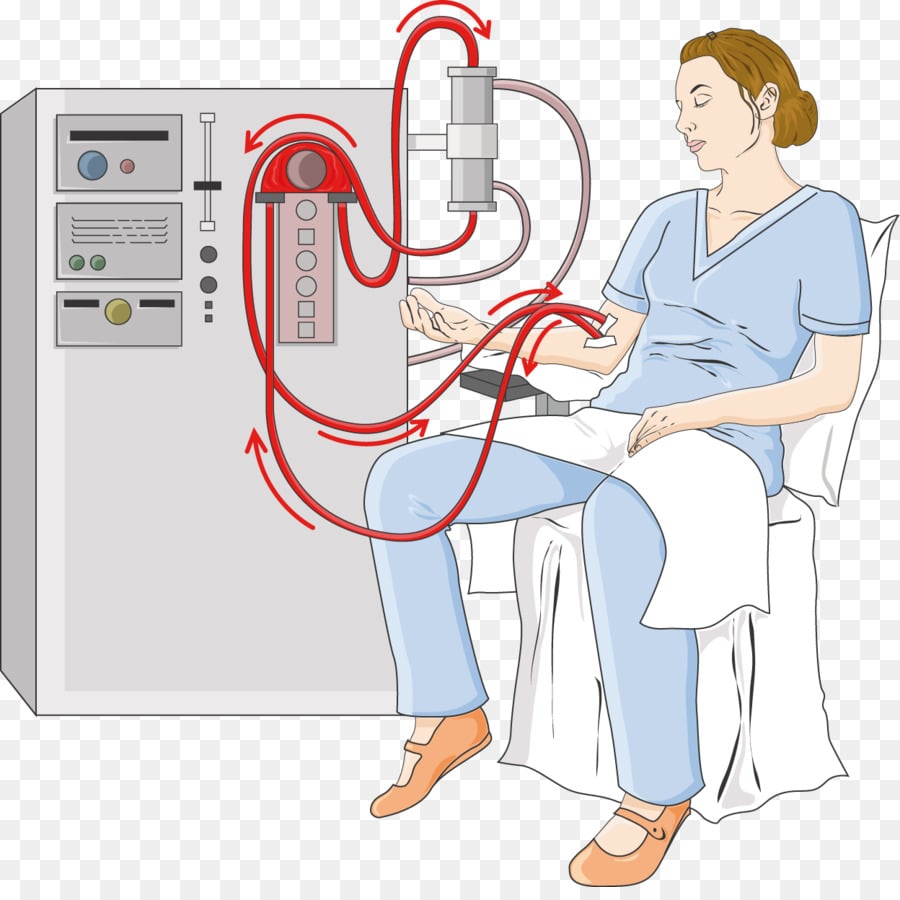
En la hemodiálisis, la sangre es bombeada a través de tubos blandos hacia la máquina de diálisis. Dentro del equipo hay un filtro especial llamado dializador o riñón artificial. El dializador deja circular los desechos y el líquido adicional, y retiene las cosas importantes que necesita el cuerpo, como células sanguíneas y nutrientes.
Se ha observado sobredosis accidentales cuando se han administrado dosis elevadas a pacientes con insuficiencia. Los síntomas de una sobredosis son encefalopatía que se manifiesta con alteraciones de la consciencia como alucinaciones, estupor, confusión y coma, mioclonía y convulsiones.
Embarazo y lactancia
Durante las investigaciones del fármaco, no se ha observado reducción de la fertilidad en ratas. En cuanto a la fertilidad humana no hay datos acerca del efecto de cefepima.
En estudios reproductivos realizados en ratones, conejos y ratas no demostraron reportes de daños
fetal, sin embargo, no existen estudios adecuados y bien controlados que certifiquen los efectos en las mujeres embarazadas.
Los estudios de reproducción en animales, generalmente no son predictivos de la respuesta en humanos, por lo tanto, este fármaco debe usarse con precaución durante la gestación sólo si es absolutamente necesario.
En el caso de la lactancia, la cefepima se excreta en la leche materna en concentraciones muy bajas. Por ende, debe tenerse precaución cuando se administre a dosis a mujeres lactantes.
Capacidad para conducir y utilizar máquinas
No se han detectados efectos del fármaco, sobre la capacidad para conducir y utilizar máquinas. La cefepima ha producido reacciones adversas, como estado alterado de conciencia, mareos, confusión pueden alterar la capacidad para conducir y utilizar máquinas. Por lo tanto, por las posibles reacciones adversas, se debe mantener las precauciones sobre la capacidad para conducir y utilizar máquinas.
Actualizado el 12 abril, 2024